Spis treści
Trzy dekady badań bez leku na alzheimera
Na temat choroby Alzheimera wciąż pisze się, że jej przyczyna jest nieznana. Tymczasem już od lat naukowcy wskazywali na procesy autoimmunologiczne, czyli z autoagresji. Tak mówi się w sytuacjach, gdy organizm błędnie rozpoznaje jako obce, atakuje i niszczy własne tkanki.
Sprawdź: Cholesterol całkowity i trójglicerydy mogą wskazywać na ryzyko alzheimera
Tak dzieje się również w innych schorzeniach autoimmunologicznych, których jest ponad osiemdziesiąt – jak choroba Hashimoto, cukrzyca typu 1, łuszczyca, atopowe zapalenie skóry, reumatoidalne zapalenie stawów, stwardnienie rozsiane, toczeń rumieniowaty, choroba Leśniowskiego-Crohna, wrzodziejące zapalenie jelita grubego czy celiakia.
Diagnozę o chorobie Alzheimera co trzy sekundy słyszy jedna osoba na świecie. Niestety, w Polsce we wczesnej fazie rozwoju rozpoznaje się ją tylko u 1 na 5 pacjentów. Choć liczbę chorych szacuje się w kraju na przeszło 580 tys. osób, według dostępnych danych (z 2019 r.) z opieki finansowanej przez NFZ skorzystało tylko 236,3 tys. pacjentów ze zdiagnozowanym schorzeniem.
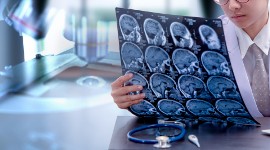
W przebiegu alzheimera dochodzi do uszkodzeń mózgu przez złogi beta-amyloidu, co skutkuje stopniową utratą jego funkcji. Do tej pory proponowano różne teorie na temat mechanizmu tego zjawiska. Tym samym badaczom umykała skuteczna terapia choroby.
Pomimo przeszło dwustu badań klinicznych w przeprowadzonych w ciągu ostatnich 30 lat do niedawna nie było środków modyfikujących przebieg choroby, które umożliwiłyby jej zapobieganie, zatrzymanie postępu czy tym bardziej skuteczne leczenie.
Alzheimer jako przewlekła choroba autoimmunologiczna
Nowy model mechanizmu rozwoju choroby Alzheimera zaproponowali badacze z Krembil Brain Institute, który jest częścią sieci szpitali badawczych University Health Network. Zaproponowali oni, by postrzegać problem nie jako chorobę mózgu, tylko przewlekłą chorobą autoimmunologiczną, która atakuje mózg. Model jej przedstawili opisali na łamach pisma „Alzheimer's & Dementia”.
– Nie uważamy alzheimera za chorobę mózgu, tylko układu odpornościowego w mózgu – powiedział dr Donald Weaver, autor badania i współdyrektor Krembil Brain Institute. – Potrzebne są nam nowe sposoby myślenia na temat choroby, i to jak najszybciej. Do tej pory większość badań na temat alzheimera bazowała na teorii mówiącej o tym, że w jej przebiegu dochodzi do zbijania się w złogi białka o nazwie beta-amyloid, który jest przypuszczalnie anormalny w mózgu. Gdy zachodzą te procesy, komórki mózgowe umierają. My wierzymy jednak, że beta-amyloid jest dokładnie tam, gdzie powinien być. Pełni bowiem rolę immunopeptydu – posłańca informacji wewnątrz układu odpornościowego. Jeśli więc mamy np. uraz głowy, beta-amyloid naprawia zniszczenia. Jeśli pojawi się wirus lub bakteria, jest tam, by je zwalczyć.
Tu właśnie pojawia się problem:
– Gdy beta-amyloid nie może rozpoznać i rozróżnić patogenów od komórek nerwowych, atakuje własne neurony. Właśnie w ten sposób rozwija się choroba autoimmunologiczna – dodaje badacz.
Zespół badawczy pod kierownictwem dr Donalda Weavera dokonał wyczerpującego przeglądu badań, włączając w to publikacje naukowe, historie pacjentów i własne prace. Opracowany przez nich model rozwoju choroby, który nazwano AD2, uwzględnia proponowane wcześniej mechanizmy (w tym szkodliwość białek, toksyczność w stosunku do synaps nerwowych i mitochondriów, czyli centrów energetycznych komórek). Jednocześnie traktuje jednak beta-amyloid jako część większego procesu, którego składowe charakteryzują się szeregiem wzajemnych zależności.
W ramach modelu rozwoju choroby Alzheimera zwrócono uwagę na dwa naturalne aminokwasy jako wewnętrzne regulatory odporności – jest to L-tryptofan i L-arginina. Wskazuje to na możliwość stworzenia nowych metod diagnostycznych i terapeutycznych.
Przeciwciała w walce z chorobą Alzheimera
O tym, że immunologiczne podejście do terapii alzheimera jest właściwe, świadczą sukcesy nowego leku na tę chorobę o nazwie Lecanemab. Składnikiem aktywnym leku jest przeciwciało monoklonalne, czyli wywodzące się z jednego rodzaju limfocytu B, co zapewnia wszystkim jego kopiom wysoką specyficzność działania.
Lek przeszedł właśnie z sukcesem 3. fazę badań klinicznych. Działa na zasadzie zakłócania tworzenia płytki beta-amyloidowej, spowalniając w ten sposób zmiany w mózgu nawet o 27 procent. W Stanach Zjednoczonych, gdzie jest opracowywany, może stać się dostępny dla pacjentów już na początku 2023 r., natomiast w Europie może się to udać przed końcem roku.
Warto wspomnieć, że również inne koncerny biofarmaceutyczne opracowują swoje leki na bazie przeciwciał monoklonalnych. Jeden z nich, aducanumab firmy Biogen, został nawet zatwierdzony w 2021 r. przez FDA, co zbudziło kontrowersje ze względu na brak wystarczających dowodów odnośnie skuteczności i bezpieczeństwa leku. Z tego powodu EMA odmówiła jego zatwierdzenia. Innych propozycji dla pacjentów wkrótce będzie jednak więcej.
Źródło: New model of Alzheimer's as an autoimmune disease University Health Network